Содержание
заполните таблицу пожалуйста. ледовое побоище дата место противоборствующие силы исход битвы значение победы — Спрашивалка
заполните таблицу пожалуйста. ледовое побоище дата место противоборствующие силы исход битвы значение победы — Спрашивалка
ВК
Виктор Куликов
- место
- значение
- дата
- сила
- таблица
- битва
- победа
- исход
Яна
Ледо́вое побо́ище, также битва на Чудском озере — битва новгородцев и владимирцев под предводительством Александра Невского против рыцарей Ливонского ордена, на льду Чудского озера, произошедшая 5 апреля 1242 года. войска тевтонского ордена были окружены русскими и уничтожены В 1243 году Тевтонский орден заключил мирный договор с Новгородом и официально отказался от всех претензий на русские земли. Несмотря на это через десять лет тевтонцы попытались вновь захватить Псков. Войны с Новгородом продолжились.
Несмотря на это через десять лет тевтонцы попытались вновь захватить Псков. Войны с Новгородом продолжились.
Катя Воронцова
Весна 1242 года, берег Чудского озера.
Дружины князей Александра и Андрея Ярославичей, новгородское и суздальское ополчения.
Бывшие меченосцы, которым не нравилось, что их перевели в Тевтонский орден, датские рыцари, Дерптское ополчение, вероятно — боевые отряды ливов и лэттов.
Князь Ярослав Владимирович был окончательно лишён шансов занять псковский стол. Ливонцы и датчане, грабившие окрестности Пскова и Новгорода были изгнаны. Александр Невский получил политический бонус — Тевтонский орден, хотя и не организовывал вторжение, вынужден был принести извинения.
Елена
литовци, а именно ливонский орден и князь александр невский под псковом в 1242 году
Марина
Смотри здесь:
http://ru.wikipedia.org/wiki/Ледовое_побоище
Тут всё подробно описано.
Юл
Юлия
ужас
СН
Сергей Новиков
Ледовое побоище
5 апреля 1242 год
лед Чудского озера
Датчане и Немцы V/S Русские
Закончилось полным разгромом Немецкого войска
Много членов ордена было убито и взято в плен остальные бежали но провалились под растаявший лед.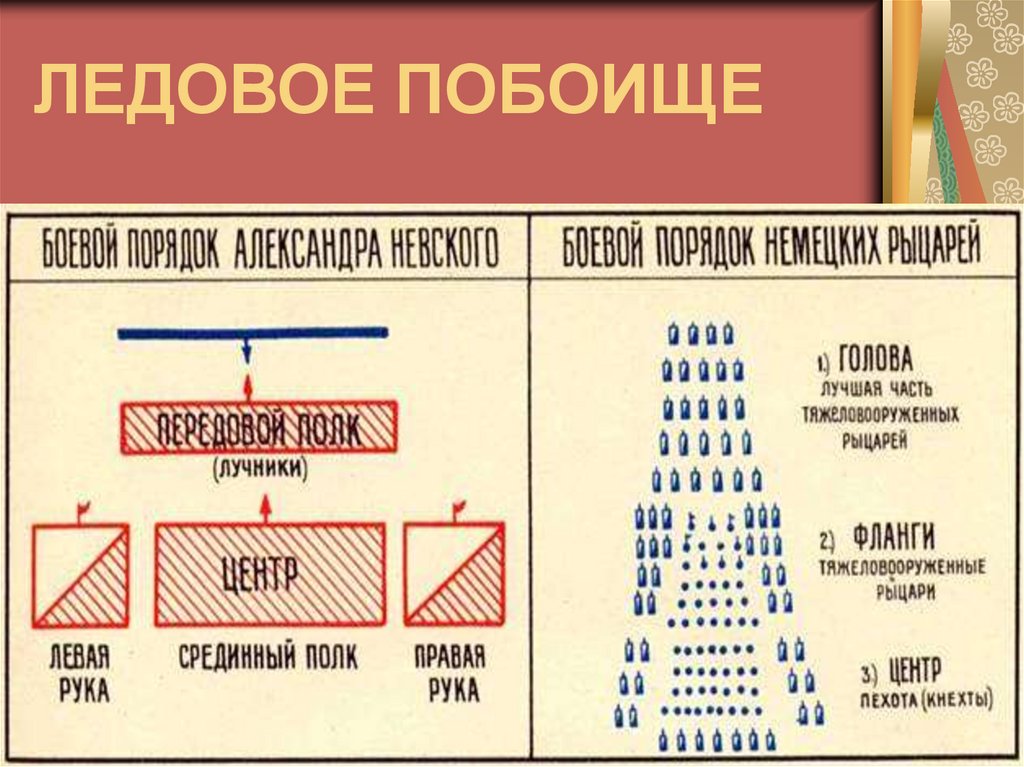
Похожие вопросы
заполнить таблицу внешняя политика бориса годунова нужна дата событие значение
когда произошла невская битва и ледовое побоище?В чем их историческое значение?
Помогите пожалуйста заполнить таблицу по химии, фотография таблици внутри
В чем историческое значение победы в битве под Москвой?
Сталинградская битва. Подскажите, пожалуйста, даты двух периодов Сталинградской битвы
Заполните таблицу Невская битва. ДатаМестоПротивоборствующие силыИсход битвыЗначение победы
Невская битва. Дата: Место: Противо- борствующие силы: Исход битвы: Значение победы:
В чем причины Невской битвы и Ледового побоища. В чем историческое значение этих битв???
Помогите пожалуйста! заполнить таблицу, образовав степени сравнения имен прилагательных.
невкая битва, битва на калке, ледовое побоище куликовская битва. какое сражение отличаетья от 3х остальных и почему?
Приложение V. Хронологическая таблица, Святой благоверный великий князь Александр Ярославич Невский
протоиерей Михаил Хитров
Святой благоверный великий князь Александр Ярославич Невский
Приложение IV. Святой Александр Невский в суждениях и отзывах русских историковИсточники, пособия
Святой Александр Невский в суждениях и отзывах русских историковИсточники, пособия
Скачать
epub
fb2
| I. События из жизни святого Александра | |
| Год рождения св. Александра Невского | 1219 |
| Начало княжения в Новгороде | 1228 |
| Самостоятельное княжение | 1236 |
| Брак | 1239 |
| Нашествие шведов | 1240 |
| Ледовое побоище и походы на Литву | 1242 |
| Походы на Литву и поражение литовцев у озера Жизца | 1245 |
| Кончина вел. кн. Ярослава | 1246 |
| Путешествие к Батыю и к истокам Амура | 1246–1250 |
| Пленение Неврюево | 1252 |
| Александр – великий князь | 1252 |
| Посольство папы | 1252 |
| Набег литовцев и их поражение близ Торопца | 1253 |
| Изгнание новгородцами Василия Александровича | 1253 |
| Финляндский поход | 1256 |
| Переговоры с татарами относительно дан | 1253–1257 |
| Новая распря с Новгородом из-за дан | 1257–1259 |
| Рождение Даниила | 1261 |
Поход Ярослава и Димитрия против немцев. Взятие Юрьева Взятие Юрьева | 1262 |
| Последнее путешествие в орду и кончина св. Александра | 1263 |
| II. События в Юго-Западной Руси | |
| Вступление на престол Даниила Романовича | 1229 |
| Путешествие Даниила в Орду | 1250 |
| Коронование Даниила в Дрогичине королевским венцом | 1255 |
| Кончина Даниила | 1264 |
| Мученическая кончина в Орде Михаила черниговского | 1246 |
| III. Монголы | |
| Чингиз-хан | 1154–1227 |
| Разорение царства гангутов | 1206 |
| Поход на Ховарезм (Бухару) | 1219 |
| Битва на Калке | 1224 |
| Окончательное покорение Тангута и сев. Китая | 1227 |
| Опустошение Рязанской области | 1237 |
| Битва при Сити | 1238 |
| Взятие Киева | 1240 |
| Битва при Лигнице | 1241 |
| Погибель Багдадского халифата | 1258 |
IV. Швеция Швеция | |
| Эрик Эриксон, при фактической власти Биргера | 1216–1251 |
| Вальдемар, сын Биргера | 1251–1275 |
| V. Норвегия | |
| Гакон V | 1217–1263 |
| VI. Дания | |
| Вальдемар II Победоносный. Его супруга Дагмара, героиня народных песнопений | 1202–1241 |
| Эрик Плогпенниг | 1241–1250 |
| Абель | |
| Кристоф | ✝ 1259 |
| Эрик | 1259–1285 |
| VII. Ливонский орден | |
| Альберт | 1199–1229 |
| Основание ордена и построение Риги | 1201 |
| Падение Юрьева | 1224 |
| Соединение Ливонского и Тевтонского орденов | 1237 |
VIII. Литва Литва | |
| Крещение Миндовга | 1252 |
| Смерть | 1263 |
| IХ. Польша | |
| Лешек | 1206–1227 |
| Германизация Померании и Вендской земли между Эльбою и Одером Болеслав | |
| 1227–1238 | |
| Генрих Благочестивый | |
| Распадение Польши на 11–14 независимых владений | |
| Х. Богемия | |
| Оттокар II | 1253–1278 |
| Борьба Оттокара с Рудольфом Габсбургским | |
| XI. Венгрия | |
| Андрей II | 1205–1235 |
| Бела IV | 1235–1270 |
| XII. Византия | |
| Взятие Константинополя крестоносцами | 1204 |
| Латинская империя | 1204–1261 |
| Михаил Палеолог изгоняет латинцев | 1261 |
XIII. Германия Германия | |
| Фридрих II Гогенштауфен | 1212–1250 |
| Продолжение эпохи крестовых походов и борьбы пап с императорами | |
| Крестовый поход его | 1228–1229 |
| Конрад IV | 1250–1254 |
| Падение дома Гогенштауфенов | |
| XIV. Франция | |
| Усиление могущества Капетингов | |
| Людовик IX Святой | 1226–1270 |
| Крестовые походы Людовика | |
| Продолжение и окончание альбигойских войн | 1218–1229 |
| Составление инструкции для инквизиции на Тулузском соборе, по поручению Иннокентия III | 1229 |
| XV. Испания | |
| Войны с маврами | |
| Фердинанд III Святой | 1230–1252 |
| Альфонс X | 1252–1284 |
XVI. Англия Англия | |
| Начало установления парламентского правления | |
| Генрих III | 1216–1272 |
| XVII. Современные папы | |
| Иннокентий III | 1198–1216 |
| Гонорий III | 1216–1227 |
| Григорий IX | 1227–1241 |
| Целестин IV, умер. без посвящения | |
| Иннокентий IV | 1243–1254 |
| Александр IV | 1254–1261 |
| Урбан IV | 1261–1265 |
Приложение IV. Святой Александр Невский в суждениях и отзывах русских историковИсточники, пособия
Источник: Святой Александр Невский / Хитров М.И. — М.: Терра : Кн. клуб Книговек — 2014. — 320 с.
Таблицы ICE — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 1348
Таблица ICE ( I nitial, C hange, E quilibrium) представляет собой простой матричный формализм, который используется для упрощения расчетов в обратимых равновесных реакциях (например, слабые кислоты и слабые основания или образование сложных ионов).
Введение
Таблицы ICE составлены из концентраций молекул в растворе на разных стадиях реакции и обычно используются для расчета K или выражения константы равновесия реакции (в некоторых случаях может быть задано K, а одна или несколько концентраций в таблице будут неизвестными для решения). Таблицы ICE автоматически настраивают и организуют переменные и константы, необходимые при вычислении неизвестного.
ICE — это простая аббревиатура для заголовков первого столбца таблицы.
- I обозначает начальную концентрацию . Эта строка содержит начальные концентрации продуктов и реагентов.
- C означает изменение концентрации . Это изменение концентрации, необходимое для достижения равновесия реакции. Это разница между равновесным и исходным рядами. Концентрации в этой строке, в отличие от других строк, выражены либо соответствующим положительным (+), либо отрицательным (-) знаком и переменной; это потому, что эта строка представляет собой увеличение или уменьшение (или отсутствие изменений) концентрации.

- E для концентрации, когда реакция находится в состоянии равновесия . Это суммирование начального и итогового рядов. Как только эта строка заполнена, ее содержимое можно подставить в уравнение константы равновесия, чтобы найти \(K_c\).
Процедуру заполнения таблицы ICE лучше всего проиллюстрировать на примере.
Пример 1
Используйте таблицу ICE для определения \(K_c\) для следующей сбалансированной общей реакции:
\[ \ce{ 2X(г) <=> 3Y(г) + 4Z(г)} \номер\]
где заглавные буквы обозначают продукты и реагенты.
- Это уравнение будет размещено горизонтально над таблицей, где каждый продукт и реагент будут иметь отдельный столбец.
Образец, состоящий из 0,500 моль х, помещают в систему объемом 0,750 л.
- Это утверждение подразумевает, что начальных количеств Y и Z нет. Для строки I столбцов Y и Z будет введено 0,000 моль.
- Обратите внимание, что исходный состав указан в молях.
 Количества могут быть либо преобразованы в концентрации перед помещением их в таблицу ICE, либо после расчета равновесных количеств. В этом примере для таблицы ICE используются моли, а концентрации рассчитываются позже.
Количества могут быть либо преобразованы в концентрации перед помещением их в таблицу ICE, либо после расчета равновесных количеств. В этом примере для таблицы ICE используются моли, а концентрации рассчитываются позже.
Известно, что в равновесии количество образца x составляет 0,350 моль.
- Для строки равновесия X будет введено 0,350 моль.
Желаемый Неизвестный 92} \nonumber \]
Равновесные концентрации Y и Z неизвестны, но их можно рассчитать с помощью таблицы ICE.
ШАГ 1: Введите указанные суммы
| Реакция: | 2X | 3 года | 4З |
|---|---|---|---|
| Начальные суммы | 0,500 моль | 0,000 моль | 0,000 моль |
| Изменение суммы | ? | ? | ? |
| Равновесная сумма | 0,350 моль | ? | ? |
Это первый шаг в настройке таблицы ICE. Как упоминалось выше, мнемоника ICE является вертикальной, а уравнение возглавляет таблицу горизонтально, задавая строки и столбцы таблицы соответственно. Были даны численные суммы. Любая сумма, не указанная напрямую, неизвестна.
Как упоминалось выше, мнемоника ICE является вертикальной, а уравнение возглавляет таблицу горизонтально, задавая строки и столбцы таблицы соответственно. Были даны численные суммы. Любая сумма, не указанная напрямую, неизвестна.
ШАГ 2: Введите сумму изменения для каждого соединения
| Реакция | 2X | 3 года | 4З |
|---|---|---|---|
| Начальные суммы | 0,500 моль | 0,000 моль | 0,000 моль |
| Изменение суммы | -0,150 моль | +0,225 моль | +0,300 моль |
| Равновесные суммы | 0,350 моль | ? | ? |
Обратите внимание, что равновесие в этом уравнении смещено вправо, что означает удаление некоторого количества реагента и добавление некоторого количества продукта (для строки Изменение).
Изменение суммы (\(x\)) можно рассчитать с помощью алгебры:
\[ Равновесие \; Сумма = Начальная \; Сумма + Сдача \; в \; Сумма \номер\]
Решение для изменения суммы \(2x\) дает:
\[ 0,350 \; моль — 0,500\; моль = -0,150 \; моль \номер \]
Изменение реагентов и сбалансированное уравнение реакции известны, поэтому можно рассчитать изменение продуктов. Стехиометрические коэффициенты показывают, что на каждые 2 моля прореагировавшего x образуется 3 моля Y и 4 моля Z. Соотношение следующее:
\[ \begin{eqnarray} Изменить \; в \; Продукт &=& -\left(\dfrac{\text{Стехиометрический коэффициент продукта}}{\text{Стехиометрический коэффициент реагента}}\right)(\text{Изменение реагента}) \\ Изменение \; в \; Y &=& -\left(\dfrac{3}{2}\right)(-0,150 \; моль) \\ &= +0,225 \; mol \end{eqnarray} \nonumber \]
Попробуйте получить изменение Z этим методом (ответ уже есть в таблице ICE).
ШАГ 3: Найдите равновесные количества
| Реакция | 2X | 3 года | 4З |
|---|---|---|---|
| Начальные суммы | 0,500 моль | 0,000 моль | 0,000 моль |
| Изменение сумм | -0,150 моль | +0,225 моль | +0,300 моль |
| Равновесные суммы | 0,350 моль | 0,225 моль | 0,300 моль |
Если начальные количества Y и/или Z были ненулевыми, то они должны быть добавлены вместе с изменением количеств для определения равновесных количеств.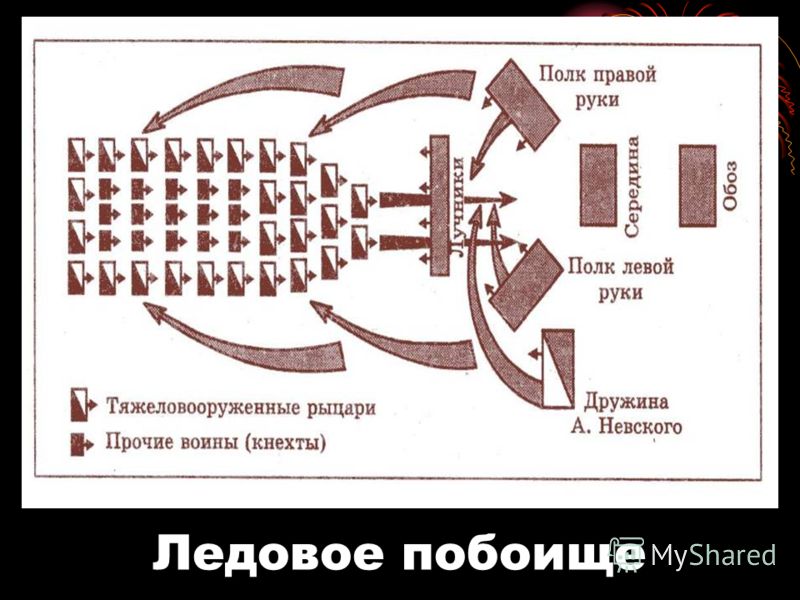 Однако, поскольку начального количества двух продуктов не было, равновесное количество просто равно изменению:
Однако, поскольку начального количества двух продуктов не было, равновесное количество просто равно изменению:
\[\begin{eqnarray} Равновесие \; Сумма &=& Исходная \; Сумма + Сдача \; в \; Сумма \\Равновесие\; Количество \; из \; Y &=& 0,000 \; моль\; + 0,225\; моль \&=&+0,225\; моль \end{eqnarray} \nonumber \]
Используйте тот же метод, чтобы найти равновесное количество Z. Преобразуйте равновесные количества в концентрации. Напомним, объем системы 0,750 л.
\[[Равновесие \; Концентрация \; из \; Вещество] = \dfrac{Количество \; из \; Вещество}{Объем \; из \; Система}\номер\] 9{-3} \end{eqnarray}\nonumber \]
Пример 2: Использование таблицы ICE с концентрациями
В этом примере таблица ICE используется для определения равновесной концентрации реагентов и продуктов. (Этот пример будет менее подробным, чем предыдущий, но применяются те же принципы.) Эти расчеты часто выполняются для титрования слабыми кислотами.
Найдите концентрацию A — для общей реакции диссоциации кислоты:
\[ \ce{HA(водн. {+} (водный)} \номер\] 9-\)) и протоны (Н 3 О + ). Обратите внимание, что вода является жидкостью, поэтому ее концентрация не имеет отношения к этим расчетам.
{+} (водный)} \номер\] 9-\)) и протоны (Н 3 О + ). Обратите внимание, что вода является жидкостью, поэтому ее концентрация не имеет отношения к этим расчетам.
ШАГ 1: Введите указанные концентрации
| Реакция: | ГА | А — | Н 3 О + |
|---|---|---|---|
| I | 0,150 М | 0,000 М | 0,000 М |
| С | ? | ? | ? |
| Е | ? | ? | ? |
- Содержимое крайнего левого столбца сокращено для удобства.

ЭТАП 2: Рассчитайте изменение концентрации с помощью переменной «x»
| Реакция: | ГА | А — | Н 3 О + |
|---|---|---|---|
| я | 0,150 М | 0,000 М | 0,000 М |
| С | -х М | +х М | +х М |
| Е | ? | ? | ? |
- Изменение концентрации неизвестно, поэтому для обозначения изменения используется переменная x.
 x одинаков как для продуктов, так и для реагентов, поскольку равные стехиометрические количества A — и H 3 O + образуются при диссоциации ГК в воде.
x одинаков как для продуктов, так и для реагентов, поскольку равные стехиометрические количества A — и H 3 O + образуются при диссоциации ГК в воде.
ЭТАП 3: Расчет концентраций при равновесии
| Реакция: | ГА | А — | Н 3 О + |
|---|---|---|---|
| я | 0,150 М | 0,000 М | 0,000 М |
| С | -х М | +х М | +х М |
| Е | 0,150 — х М | х М | х М |
- Чтобы найти равновесные суммы, складывают строки I и строки C.
 Используйте эти значения и K 92-4AC}}{2A}\nonumber \]
Используйте эти значения и K 92-4AC}}{2A}\nonumber \]Чтобы определить правильное решение, следует использовать интуицию. Если дать отрицательную концентрацию, ее можно устранить, потому что отрицательная концентрация нефизична.
Значение x можно использовать для расчета равновесных концентраций каждого продукта и реагента, подставив его в элементы в строке E ледяной таблицы.
[Решение: х = 0,0416, -0,0576. x = 0,0416 имеет химический смысл и, следовательно, является правильным ответом.]
Для некоторых задач, таких как пример 2, если x значительно меньше значения для K a , тогда x реагентов (в знаменателе) можно опустить, и концентрация для x не должна сильно повлиять. Это ускорит расчеты, избавив от необходимости использовать квадратную формулу.
Контрольный список для таблиц ICE
- Убедитесь, что обратимое уравнение сбалансировано в начале задачи; в противном случае в таблице будут использованы неправильные суммы.

- Приведенные данные должны быть в количествах, концентрациях, парциальных давлениях или каким-либо образом быть преобразованы в такие. Если это не так, то таблица ICE не поможет решить проблему.
- Если в таблице ICE есть равновесные количества , убедитесь, что равновесные значения преобразованы в концентрации перед подключением для решения \(K_c\).
- Если данные представлены в виде количеств или концентраций, используйте таблицу ICE, чтобы найти \(K_c\). Если данные находятся в 9{\Delta n_{gas}}\nonumber \] Проще использовать таблицу ICE с соответствующими данными и конвертировать в конце задачи.
- Введите в сначала известные данные , а затем вычислите неизвестные данные.
- Если в строках «начальная» или «равновесная» имеется отрицательное значение, перепроверьте расчет. Отрицательная концентрация, количество или парциальное давление физически невозможны.
 Очевидно, что строка «изменение» может содержать отрицательное значение.
Очевидно, что строка «изменение» может содержать отрицательное значение. - Обратите внимание на состояние каждого реагента и продукта. Если соединение является твердым или жидким, его концентрации не имеют отношения к расчетам. Используются только концентрации газообразных и водных соединений.
- В строке «изменение» значения обычно представляют собой переменную, обозначаемую как x . Прежде всего необходимо понять, в каком направлении уравнение придет к равновесию (слева направо или справа налево). Значение «изменения» в направлении «от» реакции будет противоположно 9.0582 x , а направление «к» будет положительным от x (добавляя концентрацию с одной стороны и убирая такое же количество с другой стороны).
- Знать направление реакции . Это знание повлияет на строку «изменение» таблицы ICE (в нашем примере мы знали, что реакция будет продолжаться, так как исходных продуктов не было). Направление реакции можно рассчитать, используя коэффициент реакции Q, который затем сравнивают с известным значением K.

- Проще всего использовать одни и те же единицы каждый раз, когда используется таблица ICE (обычно предпочтительна молярность). Это сведет к минимуму путаницу при расчете констант равновесия. Таблицы ICE обычно используются для слабокислотных или слабоосновных реакций из-за всей природы этих растворов. Количество кислоты или основания, которое диссоциирует, неизвестно (для сильных кислот и сильных оснований можно предположить, что диссоциирует вся кислота или основание, а это означает, что концентрация сильной кислоты или основания такая же, как и у ее диссоциированных частиц). .
Парциальные давления также могут быть заменены на концентрации в таблице ICE, если это необходимо (т.е., если концентрации не известны, требуется \(K_p\) вместо \(K_c\) и т. д.). «Количество» также допустимо (таблица ICE может быть выполнена в количествах до тех пор, пока не будут найдены равновесные количества, после чего они будут преобразованы в концентрации).
 Для простоты предположим, что слово «концентрация» можно заменить на «парциальное давление» или «количества» при составлении таблиц ICE. 9{-6}\)?
Для простоты предположим, что слово «концентрация» можно заменить на «парциальное давление» или «количества» при составлении таблиц ICE. 9{-6}\)?- Ответить
5,99×10 -4
Упражнение \(\PageIndex{2}\)
Если начальная концентрация NH 3 равна 0,350 М, а равновесная концентрация равна 0,325 М, чему равно \(K_c\) для этой реакции?
- Ответить
1,92×10 -3
Упражнение \(\PageIndex{3}\)
Как получается \(K_c\) из \(K_p\)? 9{\Delta n}\), затем найдите \(K_c\)
Упражнение \(\PageIndex{4}\)
Заполните эту таблицу ICE:
Реакция: [ГА] [А — ] [Н 3 О + ] я 0,650 моль ? ? С ? ? ? Е 0,250 моль ? ? - Ответить
Реакция: ГА А- Н 3 О + я 0,650 моль 0,000 моль 0,000 моль С -0,400 моль +0,400 моль +0,400 моль Е 0,250 моль 0,400 моль 0,400 моль
Авторы и ссылки
- Александр Шей (UCD), Эйлин Макдафф (UCD)
ICE Tables распространяется по лицензии CC BY, автор, ремикс и/или куратор LibreTexts.

- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- СС BY
- Показать страницу TOC
- № на стр.
- Теги
- Стол для льда
Таблица эффективности и слабости типов Pokémon Go
Таблица типов методов представления Эффективность типов были популярны задолго до Pokémon Go, и все основные игры Pokémon вращались вокруг них.

Вкратце, типы покемонов определяют, является ли один покемон сильным или слабым, суперэффективным или не очень эффективным против другого, нанося в результате дополнительный или уменьшенный урон и получая в результате дополнительный или уменьшенный урон.
Стандартная таблица типов, которая развивалась на протяжении разных поколений, будет как второй язык для давних поклонников покемонов, но для новичков она может показаться слишком сложной, чтобы даже знать, с чего начать, поэтому, имея это в виду, мы добавили вместе нашу собственную диаграмму типов, а также объяснение того, как работает эффективность типов и как спланировать ее, чуть ниже.
На этой странице:
- Таблица типов, объяснение эффективности и слабости в Pokémon Go
- Изменения эффективности типа Pokémon Go по сравнению с другими играми Pokémon
Смотреть на YouTube
Таблица типов, эффективность и слабость объясняются в Pokémon Go. устойчивые атаки имеют немного другие множители, чем в основных играх про покемонов, хотя обновление от декабря 2018 года немного приблизило их в соответствие.

Вот таблица типов Pokémon Go, чтобы вы могли понять, что против чего эффективно.
Type Strong Against Weak Against Resistant To Vulnerable To Normal Rock, Ghost, Steel Ghost Fighting Боевой Обычный, Каменный, Стальной, Ледяной, Тёмный Полёт, Ядовитый, Психический, Жук, Призрак, Фея Каменный, Жук, Тёмный Полёт, Психический, Фея Полет Бой, Баг, Грава Скала, сталь, электрический , земля, баг, , электрический, ледяной 976, 4,
4,
, ,,,, ,,,,. Яд, Земля, Камень, Призрак, Сталь Боевой, Яд, Трава, Фея Земля, Психика Земля Яд, Камень, Сталь, Огонь, Электрические Жуки 0133 Яд, Камень, Электрический Вода, Трава, Лед Камень Полет, Насекомое, Огонь, Лед Борьба, Земля, Сталь 9093 Земля, Сталь, Вода, Трава
Жук Трава, Психика, Тьма Бой, Полет, Яд, Призрак, Сталь, Огонь, Фея Бой, Земля, Трава, Полет 63
63
3
Призрак Призрак, Психис Нормальный, темный Нормальный, борьба, яд, Bug Призрак, Стиль Стиль Стиль .  , Электрический
, ЭлектрическийОбычный, Летающий, Ядовитый, Каменный, Жук, Стальной, Травяной, Психический, Ледяной, Драконий, Фея Боевой, Земляной, Огонь Огонь Жук, Стальной, Травяной, Ледяной 3 Камень, Огонь, Вода, Дракон
Жук, Сталь, Огонь, Трава, Лед Земля, Камень, Вода Вода Земля, Камень, Огонь Вода, Трава, Дракон 9 Вода, Огонь, Сталь Трава, электричество
Трава Земля, камень, вода Летающий, яд, жук, сталь, огонь, трава, дракон Земля, вода, трава, электричество Летающий, жук , Лед Electric Flying, Water Ground, Grass, Electric, Dragon Flying, Steel, Electric Ground Psychic Fighting, Poison Steel, Psychic, Dark Fighting , Психика Жук, Призрак, Тьма Лед Полет, Земля, Трава, Дракон Сталь, Огонь, Вода, Лед Лед, Огонь Сталь, Скалы 0133 Dragon Dragon Steel, Fairy Fire, Water, Grass, Electric Ice, Dragon, Fairy Fairy Fighting, Dragon, Dark Poison, Steel , Огонь Боевой, Жук, Дракон, Тьма Яд, Сталь Тьма Призрак, Психика Боевой, Тьма, Фея Psychic, Призрак
0976 Борьба, Жук, Фея Сезон Mythical Wishes продолжается событием Winter Holiday, которое принесло Mega Glalie в Pokémon Go.
 Не забудьте принять участие в новом сезоне Go Battle League.
Не забудьте принять участие в новом сезоне Go Battle League.В других местах обязательно используйте благовония Daily Adventure, чтобы получить шанс встретить Галариана Артикуно, Галариана Запдоса и Галариана Молтреса.
Изменения эффективности типа Pokémon Go по сравнению с другими играми Pokémon
Как вы могли заметить, в Pokémon Go также нет иммунитета к Типу, в отличие от основной серии. Но это еще не все. Удаленные иммунитеты:
- Невосприимчивость к земле к электричеству
- Летающий иммунитет к Земле
- Призрак невосприимчив к нормальному и боевому
- Нормальный и Боевой иммунитет к Призраку
- Сталь невосприимчива к яду
- Темный иммунитет к психическому
- Фея с иммунитетом к дракону
Вместо полного иммунитета к урону они изначально работали так же, как и простые сопротивления. Теперь, однако, они были изменены, чтобы сформировать еще один уровень сопротивления: защищающиеся покемоны, которые обычно невосприимчивы, получают всего 0,39.

- Убедитесь, что обратимое уравнение сбалансировано в начале задачи; в противном случае в таблице будут использованы неправильные суммы.

 Количества могут быть либо преобразованы в концентрации перед помещением их в таблицу ICE, либо после расчета равновесных количеств. В этом примере для таблицы ICE используются моли, а концентрации рассчитываются позже.
Количества могут быть либо преобразованы в концентрации перед помещением их в таблицу ICE, либо после расчета равновесных количеств. В этом примере для таблицы ICE используются моли, а концентрации рассчитываются позже.
 x одинаков как для продуктов, так и для реагентов, поскольку равные стехиометрические количества A — и H 3 O + образуются при диссоциации ГК в воде.
x одинаков как для продуктов, так и для реагентов, поскольку равные стехиометрические количества A — и H 3 O + образуются при диссоциации ГК в воде. Используйте эти значения и K 92-4AC}}{2A}\nonumber \]
Используйте эти значения и K 92-4AC}}{2A}\nonumber \]
 Очевидно, что строка «изменение» может содержать отрицательное значение.
Очевидно, что строка «изменение» может содержать отрицательное значение.
 Для простоты предположим, что слово «концентрация» можно заменить на «парциальное давление» или «количества» при составлении таблиц ICE. 9{-6}\)?
Для простоты предположим, что слово «концентрация» можно заменить на «парциальное давление» или «количества» при составлении таблиц ICE. 9{-6}\)?

